目次
肝細胞がんとは
肝臓は腹部の右上にある体内で最大の臓器です。肝細胞がんとは、肝臓の細胞ががん化して悪性腫瘍になったものです。但し、肝臓にできたがんでも肝臓の中を通る胆管ががん化したものは肝内胆管がん(胆管細胞がん)と呼ばれ、肝細胞がんには含まれません。一般的に、肝がんは肝細胞がんのことを言います。
肝細胞がんのリスクファクター
B・C型慢性肝炎(B型・C型肝炎ウィルスによる感染)、非アルコール性脂肪肝炎(NASH)、常習飲酒が肝細胞がんのリスクを高めると言われています。
肝細胞がんに関係する遺伝子
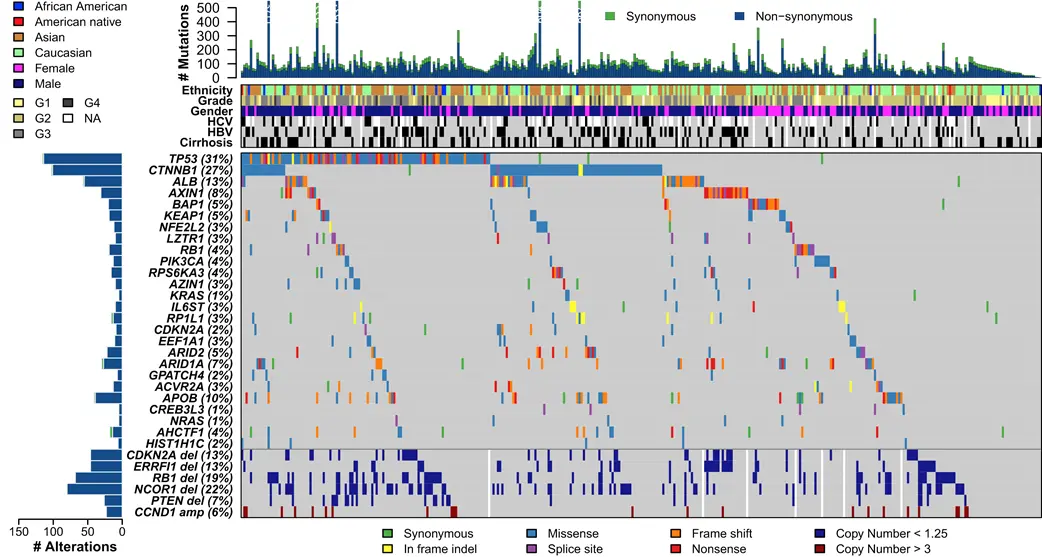
上の図は、363人の肝細胞がんの患者様について、遺伝子の本体であるDNAの中で塩基配列がタンパク質のアミノ酸配列に翻訳される領域であるエクソームの解析をおこなった結果です(3)。
左から右へ並べた個々の患者様の遺伝子の状態を左に示した項目についてまとめています。
最上段のヒストグラムは各患者様の遺伝子の変異数(緑色Synonymous:タンパク質のアミノ酸が変化しない変異、濃い青色Non-synonymous:タンパク質のアミノ酸が変化する変異)を示します。タンパク質のアミノ酸が変化する変異が多いことが分かります。
2段目から7段目は、上から患者様の人種(Ethnicity)、がんのグレード(Grade)、性別(Gender)、C型肝炎ウイルス(HCV)陽性陰性、B型肝炎ウイルス(HBV)陽性陰性、肝硬変(cirrhosis)の有無を表します。
TP53(p53)からHIST1H1Cまでは、顕著に変異している遺伝子を示します。各遺伝子の右には遺伝子変異の様式をそれぞれの患者様について以下の色で示しています。
青色
ミスセンス突然変異(Missense、タンパク質のアミノ酸が変化する変異)
オレンジ色:フレームシフト突然変異(Frame shift、タンパク質のアミノ酸を指令する塩基配列であるコドンの読み枠が変更される変異)
黄色
タンパク質のアミノ酸を指令する塩基配列であるコドンの読み枠が変更されない塩基の挿入や欠失(In-frame indel)
紫色
DNAがメッセンジャーRNAの塩基配列に転写されタンパク質のアミノ酸配列に翻訳される前には、メッセンジャーRNAの塩基配列の中でアミノ酸に翻訳されない部分が除去される(スプライシング)必要がありますが、このようなスプライシング部位に起こった変異(Splice site)
赤色
ナンセンス変異(Nonsense、タンパク質の合成が途中で止まる変異)。
下から6番目から2番目の遺伝子であるCDKN2A(p16)、ERRFl1、RB1、NCOR1、PTENは、遺伝子のコピー数が著しく減った、がんの発生に関わる遺伝子の異常を示します。一番下のCCND1は遺伝子のコピー数が著しく増えた、がんの発生に関わる遺伝子の異常を示します。
また、DNAにおいてタンパク質のアミノ酸を指令するコード領域でない領域(非コード領域)の変異として、テロメラーゼのサブユニットをコードするTERT(テロメラーゼ逆転写酵素)遺伝子のプロモーター領域において44%の患者様に変異が見られました。テロメラーゼは、DNAとタンパク質の複合体である染色体の末端(テロメア)の反復配列を伸長させることにより細胞分裂の回数を増大させる酵素で、生殖細胞、幹細胞、がん細胞などでの活性が高く、これらの細胞が細胞分裂を継続できる性質に関与しています。プロモーター領域とは、DNAからメッセンジャーRNAを転写するときに基本転写因子が結合する遺伝子の上流領域です。
肝細胞がんは3つのサブタイプに分類
DNAやRNAの様々な解析結果から、肝細胞がんは3つのサブタイプ(iClust1、iClust2、iClust3)に分類できることが分かりました。
iClust1の腫瘍は、グレードが高く、血管への浸潤があり、分化した細胞が少ないという特徴がありました。がん細胞が、正常な細胞の形態をどれくらい維持しているかを分化度と言います。 一般に分化度の低いがん細胞は、悪性度が高く活発に増殖する傾向があります。また、iClust1の腫瘍は、CDKN2A(p16)遺伝子の抑制の割合がiClust2(69%)やiClust3(63%)に比べて低い(32%)、CTNNB1遺伝子の変異の割合がiClust2(38%)やiClust3(43%)に比べて低い(12%)、TERT遺伝子のプロモーターの変異の割合が低い、TERT遺伝子の発現が低いという特徴がありました。iClust2の腫瘍は、グレードが低く、血管浸潤が少ないという特徴がありました。iClust3の腫瘍は、17番染色体の短腕の欠失に代表される染色体の不安定さの程度が高く、TP53(p53)の変異の割合が高いという特徴がありました。
肝細胞がんに関係する遺伝子の異常の割合
肝細胞がんに関係する遺伝子の異常の割合を、それぞれの遺伝子が転写・翻訳されたタンパク質の働きに従って示したのが下の図です。それぞれの遺伝子名の下の3つの四角に左から右に肝細胞がんの3つのサブタイプ(iClust1、iClust2、iClust3)ごとにその遺伝子の異常の割合を示し、各遺伝子の異常により機能が活性化された場合は赤色で、不活化された場合は青色で、その活性化・不活化の程度を色の濃さで示しています。それぞれの遺伝子が転写・翻訳されたタンパク質が他の遺伝子の発現や機能を促進する場合は→で、抑制する場合は⊥で示しています。
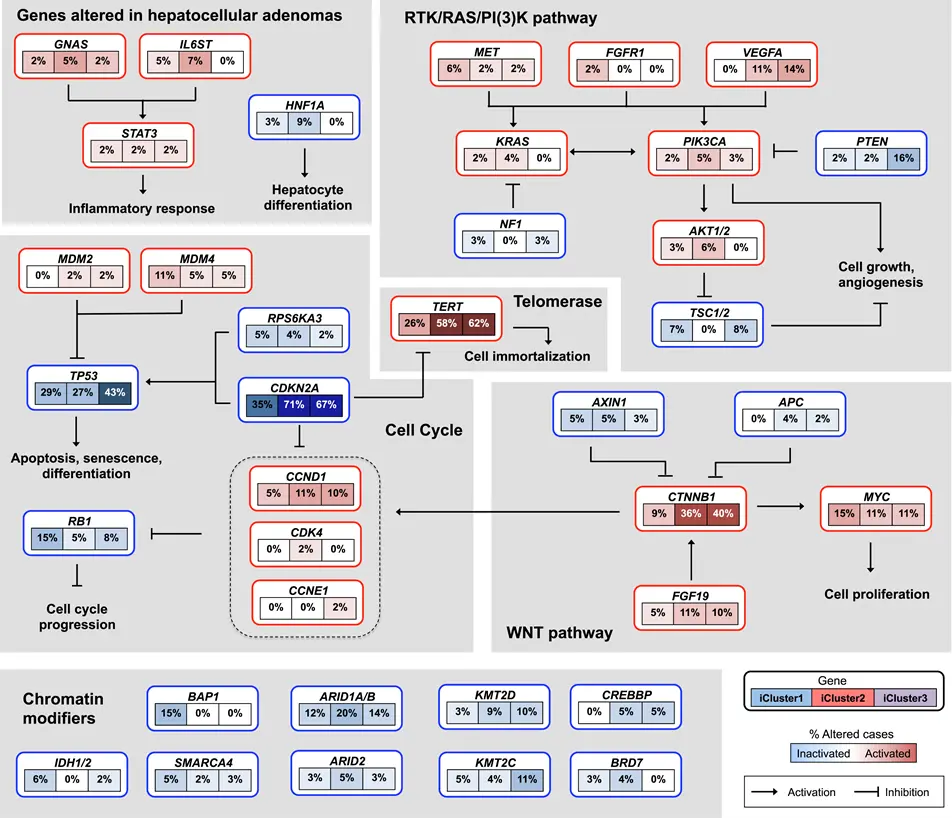
左上のグループの遺伝子(GNAS、IL6ST、STAT3、HNF1A)は、肝細胞腺腫において発現が変化する遺伝子(Genes altered in hepatocellular adenomas)で、これらの遺伝子の異常により炎症反応の活性化や肝細胞の分化の抑制が起こります。
右上のグループの遺伝子(MET、FGFR1、VEGFA、KRAS、PIK3CA、PTEN、NF1、AKT1/2、TSC1/2)は、RTK/RAS/PI3Kシグナル伝達経路(RTK/RAS/PI3K pathway)に関わる遺伝子で、これらの遺伝子の異常により細胞の成長や血管新生が促進されます。
肝細胞がんに対する全身治療として用いられるソラフェニブやレンバチニブは、RTK/RAS/PI3Kシグナル伝達経路(RTK/RAS/PI3K pathway)を抑制する分子標的薬です。
右下のグループの遺伝子(AXIN1、APC、CTNNB1、FGF19、MYC)は、WNTシグナル伝達経路(WNT pathway)に関わる遺伝子で、これらの遺伝子の異常により細胞増殖が促進されます。また、CTNNB1の活性化により左の細胞周期(Cell cycle)制御に関係する遺伝子(CCND1、CDK4、CCNE1)の機能が活性化し、細胞周期を進行させます。
左下のグループの遺伝子(BAP1、ARID1A/B、KMT2D、CREBBP、IDH1/2、SMARCA4、ARID2、KMT2C、BRD7)は、DNAとタンパク質の複合体であるクロマチンの修飾に関わる遺伝子(Chromatin modifiers)です。肝細胞がんにおいてこれらのクロマチンの修飾に関わる遺伝子は抑制される傾向があります。
左中のグループの遺伝子(MDM2、MDM4、TP53、RPS6KA3、CDKN2A、CCND1、CDK4、CCNE1、RB1)は、細胞周期(Cell cycle)に関わる遺伝子で、これらの遺伝子の異常によりプログラムされた細胞死であるアポトーシス、細胞老化(細胞周期の停止)、細胞の分化が抑制されます。また、細胞周期の進行が促進されます。さらに、CDKN2A(p16)は本来TERT(テロメラーゼ逆転写酵素)を抑制しますが、CDKN2A(p16)の機能が抑制されることによりTERT(テロメラーゼ逆転写酵素)の機能が促進され、細胞の不死化が起こります。
中にあるTERT(テロメラーゼ逆転写酵素)は、テロメラーゼ(Telomerase)のサブユニットをコードします。テロメラーゼは、DNAとタンパク質の複合体である染色体の末端(テロメア)の反復配列を伸長させることにより細胞分裂の回数を制御する酵素で、生殖細胞、幹細胞、がん細胞などでの活性が高く、これらの細胞が分裂を継続できる性質に関与しています。肝細胞がんでは、TERT(テロメラーゼ逆転写酵素)が活性化されるため細胞分裂の回数が制限されず細胞の不死化が起こります。
1.国立がん研究センターがん情報サービス 肝細胞がんについて
https://ganjoho.jp/public/cancer/liver/about.html
2.国立がん研究センター内科レジデント編 がん診療レジデントマニュアル 第8版 医学書院 2019年
3.Cancer Genome Atlas Research Network. Comprehensive and Integrative Genomic Characterization of Hepatocellular Carcinoma. Cell 2017;169:1327-1341.e23. doi: 10.1016/j.cell.2017.05.046.
https://www.cell.com/cell/fulltext/S0092-8674(17)30639-6?_returnURL=https%3A%2F%2Flinkinghub.elsevier.com%2Fretrieve%2Fpii%2FS0092867417306396%3Fshowall%3Dtrue
参照:2021年09月09日