膵臓は、胃の背側にある、長さ15cmくらいの横に細長い臓器です。十二指腸につながる右側の部分を膵頭部、中ほどを膵体部、左側の幅が狭くなっている部分を膵尾部と言い、膵尾部は脾臓に接しています。
膵臓の中には、膵管が網の目のように走っています。膵臓には、食物の消化を助ける膵液を作り十二指腸に分泌する外分泌機能と血糖値の調節などをするホルモンを作り血中に分泌する内分泌機能があります。血糖値の調節をするホルモンには、血中の糖分を減らすインスリンや血中の糖分を増やすグルカゴンがあります。
食物の消化を助ける膵液には、タンパク質分解酵素、脂質分解酵素、糖質分解酵素、核酸分解酵素が含まれています。膵液は、膵管によって運ばれ、主膵管に集まり、十二指腸乳頭で、肝臓から総胆管内を通って運ばれてきた胆汁と共に十二指腸内に排出されます。膵臓がんの多くは膵管の細胞から生じます。膵臓では、膵管内乳頭粘液性腫瘍(IPMN)や神経内分泌腫瘍なども発生することがありますが、これらは膵臓がんとは異なる疾患です。
目次
膵臓がんのリスクファクター
遺伝するリスクファクターとしては、家族性大腸腺腫症や遺伝性乳がん卵巣がん症候群などの遺伝性腫瘍症候群や遺伝性膵炎があります。合併疾患としては、糖尿病、肥満、慢性膵炎、膵管内乳頭粘液性腫瘍がリスクファクターとなります。喫煙や大量の飲酒は、生活習慣におけるリスクファクターです。
家族性膵臓がん
膵臓がん全体の内、5から10%は家族性です。日本人を対象にして行われた研究では、膵臓がん患者の約7%で、遺伝情報を50%共有する近親者である第一度近親者(親、兄弟姉妹、子ども)にすい臓がん患者がいることが明らかになりました(5)。欧米における研究では、BRCA2、BRCA1、PALB2、CDKN2A (p16)、STK11、PRSS1、ATM、MSH2、MLH1など、遺伝性乳がん卵巣がん症候群やリンチ症候群などで異常がみられる遺伝子が家族性膵臓がんの原因遺伝子とされました。
膵臓がんの遺伝子異常
下の図は、149人の膵管腺がんの患者様のがん組織において見られた遺伝子異常をまとめたものです(6)。https://www.cell.com/cancer-cell/fulltext/S1535-6108(17)30299-4
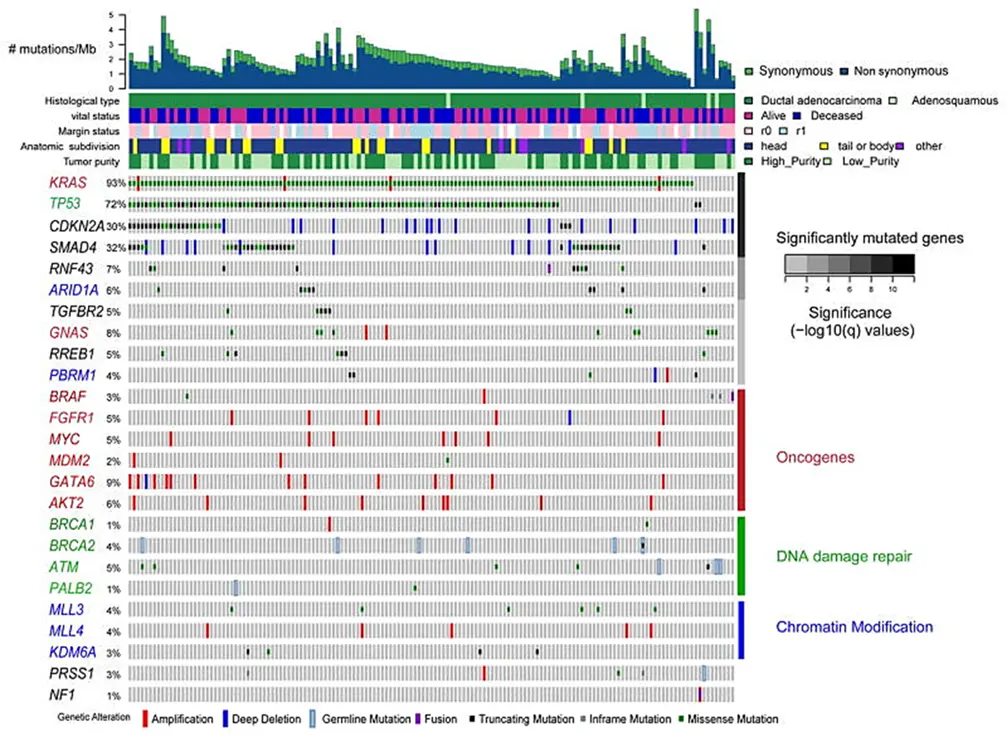
縦に並んだ長方形が一人一人の患者様の遺伝子の状態を表します。
一番上のヒストグラム(#mutation/Mb)は、遺伝子の本体であるDNAの塩基の変異の総数を表します。
DNAの塩基配列の情報は、メッセンジャーRNAに転写され、タンパク質のアミノ酸の配列に翻訳されますが、Synonymous (mutation)(緑)とはアミノ酸を変えない塩基置換であり、Non-synonymous (mutation)(青)とはアミノ酸を変える塩基置換を示します。
膵臓がんには、タンパク質のアミノ酸を変える変異(Non-synonymous mutation)が多くあることが分かります。
上から2段目は、膵臓がんの組織のタイプ(Histological type)を示しています。ほとんどすべての患者様の膵臓がんが膵管腺がん(Ductal adenocarcinoma)であり、腺扁平上皮がん(Adenosquamous carcinoma)が少数含まれていることが分かります。
5段目は、膵臓がんの膵臓における位置(Anatomical subdivision)を示しており、多くの患者様の膵臓がんは膵頭部(head)に出来、次いで膵尾部(tail)や膵体部(body)に出来ていたことが分かります。
7段目からは、上から顕著に(統計的に有意に)変異した遺伝子(Significantly mutated genes)、統計的には有意ではないが変異の見られたがん遺伝子(正常細胞のがん化を引き起こす遺伝子、Oncogenes)、DNA修復遺伝子(DNA damage repair)、クロマチン(DNAとタンパク質の複合体)修飾遺伝子(Chromatin modification)の名前を左に示しています。
がん遺伝子の名前
がん遺伝子の名前は赤色、DNA修復遺伝子の名前は緑色、クロマチン修飾遺伝子の名前は青色で示しています。各遺伝子の右の長方形には、各患者様(灰色の長方形)についてその遺伝子がどのように変化したのかを色と形(縦長の長方形、中くらいの長さの長方形、小さな四角)を重ねて示しています。
赤色の縦長の長方形(Amplification)
その遺伝子が増幅したことを示します。
青色の縦長の長方形(Deep deletion)
その遺伝子が欠失したことを示します。
水色の中抜けの縦長の長方形(Germline Mutation)
生殖細胞系列の遺伝子変異、すなわちその方が生まれながらにその遺伝子変異を持っていたことを示しています。
紫色の中くらいに縦長の長方形(Fusion)
2つの遺伝子が融合していることを示します。
黒色の小さな四角(Truncating mutation)
タンパク合成が途中で中断される変異を示します。
水色の小さな四角(Inframe Mutation)
メッセンジャーRNAのアミノ酸読み取り枠は維持される変異を示します。
緑色の小さな四角(Missense Mutation)
タンパク質中のアミノ酸が変わってしまう変異を示します。
膵臓がんで顕著な遺伝子異常
膵臓がんでは、KRAS、TP53(p53)、CDKN2A(p16)、SMAD4という4つの遺伝子に特に異常が見られることが多いことが分かりました。
KRAS
KRASは、EGFR(上皮成長因子受容体)という受容体から細胞増殖のシグナルをDNAが存在する核に伝達して、細胞増殖を進めるアクセルとしての機能を持つがん遺伝子です。
KRAS遺伝子に生じたタンパク質中のアミノ酸が変わってしまう変異や遺伝子増幅により、KRASタンパク質の機能が亢進し、細胞増殖を促進してしまうことが多くの膵臓がんの発生に関係しているものと考えられます。
TP53
次に多くのすい臓がん患者さんで異常が見られた遺伝子は、TP53という遺伝子です。TP53は、DNAを修復したり、細胞増殖を停止したり、細胞ががん化したときにアポトーシス(プログラムされた細胞死)を起こさせるがん抑制遺伝子の一つです。TP53タンパク質のアミノ酸が変わってしまったり、タンパク質合成が途中で中断したりすることによりTP53タンパク質の機能が失われることにより、細胞のがん化を止められなくなって膵臓がんが成長したことが考えられます。
CDKN2A
CDKN2Aは、細胞周期の調整に重要な役割を果たすがん抑制遺伝子です。CDKN2A遺伝子が欠失したり、CDKN2Aタンパク質のアミノ酸が変わってしまったり、タンパク質合成が途中で中断したりすることによりCDKN2Aタンパク質の機能が失われることにより、細胞周期を調節出来なくなることも膵臓がんの成長に関わることが考えられます。
SMAD4
SMAD4は、免疫細胞や幹細胞の調節や分化に関与しているトランスフォーミング増殖因子β(TGF-β)のシグナルを伝えるがん抑制遺伝子です。SMAD4遺伝子が欠失したり、SMAD4タンパク質のアミノ酸が変わってしまったり、タンパク質合成が途中で中断したりすることによりSMAD4タンパク質の機能が失われることも膵臓がんの成長に関係すると考えられます。
その他
膵臓がんでは、その他GNAS、BRAF、FGFR1、MYC、MDM2,GATA6、AKT2などのがん遺伝子に多くの患者様で遺伝子増幅が見られることも明らかになりました。
膵臓がんの発生や成長に関係する遺伝子とは
がんは、一つの遺伝子の異常で生ずるのではなく、いくつかの遺伝子の異常が積み重なって発生するものと考えられています。がん遺伝子の機能を促進させる遺伝子異常やがん抑制遺伝子の機能を失わせる遺伝子異常が生じるとがんが発生すると考えられますが、そのようながんの発生・進展に直接かかわる遺伝子をドライバー遺伝子と呼びます。上記の149人の膵臓がん患者様の遺伝子解析の結果から、膵臓がんは、KRAS、TP53、CDKN2A、SMAD4遺伝子の異常がドライバーとなって発生し、細胞が無秩序に分裂しだし、さらにDNAとタンパク質の複合体である染色体レベルの異常が生じることにより様々ながん遺伝子の増幅やがん抑制遺伝子の欠失が生じ、がんがさらに発達すると考えられます。
1.国立がん研究センター、がん情報サービス>それぞれのがんの解説>膵臓がん 基礎知識https://ganjoho.jp/public/cancer/pancreas/index.html
2.国立がん研究センター内科レジデント編、がん診療レジデントマニュアル、第8版、医学書院、2019年。
3.谷内田真一「膵臓がんのゲノム異常とそれに基づく治療戦略」、がんゲノム医療―網羅的解析からの知見と臨床応用の展望、医学のあゆみ、医歯薬出版株式会社、2020年、pp. 484-487。
4.小嶋基寛、江角浩安「膵がん」、がん生物学イラストレイテッド、第2版、羊土社、2019年、pp. 473-482。
5.Takai et al., Germline mutations in Japanese familial pancreatic cancer patients. Oncotarget. 2016; 7: 74227-74235. doi: 10.18632/oncotarget.12490.
6.Cancer Genome Atlas Research Network. Integrated Genomic Characterization of Pancreatic Ductal Adenocarcinoma. Cancer Cell. 2017; 32: 185-203. e13. doi: 10.1016/j.ccell.2017.07.007.
参照:2021年05月30日