目次
大腸がんとは
大腸は、長さ1.5から2メートルくらいの臓器で、盲腸、上行結腸、横行結腸、下行結腸、S状結腸からなる結腸と直腸S状部、上部直腸、下部直腸からなる直腸の部分に分けられます。大腸には栄養素の吸収作用はほとんどなく、小腸で消化吸収された食物の残りから水分を吸収するのがその役割です。
大腸がんは、良性のポリープががん化するものと正常な粘膜から直接発生するものとがあります。粘膜に発生したがんは、次第に大腸の壁に浸潤し、大腸の壁の外に到達すると腹腔内に散らばったり、大腸の壁のリンパ液や血液に入って、リンパ節、肝臓、肺などに転移したりします。大腸がんは、腺がん、扁平上皮がん、腺扁平上皮がんに分けられますが、大腸がんの多くは腺がんです。
大腸がんのリスクファクター
大腸腺腫(良性のポリープ)、肥満、炎症性腸疾患、糖尿病、大腸がんの家族歴(リンチ症候群や家族性大腸腺腫症を含む)、赤身肉、飲酒、喫煙は大腸がんのリスクを高めると言われています。逆に、運動、食物繊維の摂取は、大腸がんのリスクを下げると言われています。
遺伝性の大腸がん
リンチ症候群はHenry Lynchが初めて報告した大腸がんの形態です。多発性であり、若年で発症します。大腸がん以外に、子宮内膜がん、卵巣がん、胃がん、小腸がん、胆道がん、膵がん、腎盂・尿管がん、脳腫瘍なども発生しやすくなります。
リンチ症候群の主な原因は、DNA複製の際に生じた異常を修復するミスマッチ修復遺伝子の生まれながらの変異(生殖細胞系列変異)であると考えられています。ミスマッチ修復機構に異常があるとDNAの中に存在する1から数塩基の繰り返し配列であるマイクロサテライトが異常な反復を示すこと(マイクロサテライト不安定性、MSI)があるため、リンチ症候群のスクリーニングとしてマイクロサテライト不安定性の検査が行われます。リンチ症候群に関与していると考えられている4つのミスマッチ修復遺伝子(MLH1、MSH2、MSH6、PMS2)の遺伝学的検査により確定診断が行われます。
家族性大腸腺腫症(家族性大腸ポリポーシス、FAP)は、大腸ポリープが数百から数千個生じ、そこから大腸がんが発生する遺伝性の疾患です。未治療の場合平均40歳前後でがんが発症するため、大腸全摘術を行わなければがんの発症が避けられないとされています。
大腸がん以外にも、胃底部や十二指腸の多発性ポリープやがん、甲状せん乳頭がん、デスモイド腫瘍(線維性の軟部腫瘍)などの発症が見られます。家族性大腸ポリポーシスは、がん抑制遺伝子の一つであるAPC遺伝子の生まれながらの変異(生殖細胞系列変異)に新たに体細胞変異が加わることによりDNAとタンパク質の複合体である染色体の不安定性が生じ、さらに遺伝子異常が蓄積することにより大腸がんに発展すると考えられています。
大腸がんに関係する遺伝子
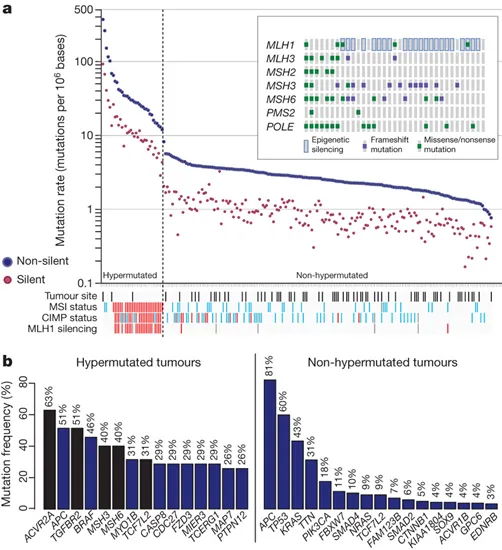
上の図は、224の大腸がんのサンプルについてどのような遺伝子に変異があるかを調べた結果です。
aのグラフにあるように、遺伝子の本体であるDNAの塩基数当たりの変異率には大きな差があり、変異が顕著な大腸がん(Hypermutated tumors)とそうでない大腸がん(Non-hypermutated tumors)に分けることが出来ました。
変異が顕著な大腸がんでは、マイクロサテライトが不安定ながん(MSI status赤)が多く見られました。マイクロサテライトとは、DNAに存在する1から数塩基の単位配列の繰り返し配列であり、DNA複製の際に生じる塩基配列の間違いを修復する機能が低下すると、マイクロサテライト配列が腫瘍組織において正常組織と異なる反復回数を示し、その遺伝子から転写翻訳されたタンパク質も不安定になりがんの原因となるのです。
また、変異が顕著な大腸がんでは、DNAミスマッチ修復タンパク質の設計図の1つであるMLH1遺伝子に遺伝子発現を抑制するDNAのメチル化が顕著でした(MLH1 silencing赤)。
変異が顕著な大腸がんでは、MLH1以外のDNA修復に関わる遺伝子(MLH3、MSH2、MSH3、MSH6、PMS2、POLE)には、それらの遺伝子から転写翻訳されるタンパク質の機能を阻害する変異が多く見られました(aの挿入図)。変異が顕著か顕著でないかに関わらず、タンパク質のアミノ酸配列に影響を与える(Non-silent)変異がタンパク質のアミノ酸配列に影響を与えない(Silent)変異より多く見られることも分かりました。
bのヒストグラムは、変異が顕著な大腸がん(Hypermutated tumors)とそうでない大腸がん(Non-hypermutated tumors)ごとに、多くのサンプルで変異が見られた遺伝子を示しています。
変異が顕著でない大腸がんでは、APC、TP53、KRAS、PIK3CA、FBXW7、SMAD4、TCF7L2、NRASなどの遺伝子に高頻度に変異が見られました。この内、がん遺伝子であるKRASとNRASに起こった変異はそれら遺伝子から転写翻訳されるタンパク質の働きを促進させる変異であり、その他の遺伝子の変異は遺伝子の機能を抑制する変異でした。変異が顕著な大腸がんでは、ACVR2A、APC、TGFBR2、BRAF、MSH3、MSH6などの遺伝子に高頻度に変異が見られました。変異が顕著でない大腸がんで高頻度に変異が見られたAPC(81%)、TP53(60%)遺伝子は、変異が顕著な大腸がんではそれほど高頻度には変異していませんでした(APC: 51%、TP53: 20%)。
大腸がんに関係する遺伝子の役割

上の図は、195の大腸がんのサンプルについておこなった遺伝子変異、遺伝子コピー数変化、遺伝子発現の解析結果に基づいて、大腸がんを生じさせる細胞内シグナル伝達の変化を明らかにしたものです。
大腸がんでは、WNTシグナル伝達(WNT signalling)、TGF-シグナル伝達(TGF- signalling)、PI3Kシグナル伝達(PI3K signalling)、RTK-RASシグナル伝達(RTK-RAS signalling)、P53シグナル伝達(P53 signalling)という細胞内シグナル伝達経路が活性化または不活化されていることが分かりました。
下段の囲みでまとめられているように、遺伝子変異が顕著でない大腸がん(Non-hypermutated tumours)でも顕著な大腸がん(Hypermutated tumours)でもWNTシグナル伝達経路、PI3Kシグナル伝達経路、RTK-RASシグナル伝達経路は活性化されており(赤)、TGF-シグナル伝達経路とP53シグナル伝達経路は不活化されていました(青)。
細胞核(Nucleus)
細胞核(Nucleus)においてDNAの塩基配列に蓄えられた遺伝子の情報はメッセンジャーRNAに転写され、メッセンジャーRNAは細胞質に出てタンパク質に翻訳されますが、あるタンパク質は細胞質で他のタンパク質の働きを促進したり(→)抑制したり(⊥)し、他のタンパク質は細胞核に入って遺伝子発現を促進したり(点々の→)抑制したり(点々の⊥)します。
WNTシグナル伝達経路
WNTシグナル伝達経路は、93%の大腸がんで活性化されていました。その理由は、APC、SOX9、TCF7L2、AXIN2、FBXW7、ARID1A、FAM123B遺伝子の不活化、CTNNB1、FDZ10遺伝子の活性化によるものでしたが、中でもAPC遺伝子の不活化が最も高頻度に見られました。
PI3Kシグナル伝達経路
PI3Kシグナル伝達経路は、50%以上の大腸がんで活性化されていました。IGF2、IRS2、PIK3CA遺伝子の活性化、PTEN、PIK3R1遺伝子の不活化がその理由でした。注目すべきは、PIK3CA遺伝子の活性化、PTEN、PIK3R1遺伝子の不活化は、相互に排他的に起こっていたことでした。
RTK-RASシグナル伝達経路
RTK-RASシグナル伝達経路の活性化は、59%の遺伝子変異が顕著でない大腸がん、80%の遺伝子変異が顕著な大腸がんで起こっていました。その内、55%の遺伝子変異が顕著でない大腸がんでは、KRAS、NRAS、BRAF遺伝子の相互に排他的な活性化が起こっていました。ERBB受容体には4つのサブタイプがありますが、13%の遺伝子変異が顕著でない大腸がん、53%の遺伝子変異が顕著な大腸がんで少なくとも1つのサブタイプで遺伝子変異または遺伝子増幅が見られました。
TGF-シグナル伝達経路
TGF-シグナル伝達経路の不活化は、27%の遺伝子変異が顕著でない大腸がん、87%の遺伝子変異が顕著な大腸がんで起こっていました。その理由は、TGFBR1、TGFBR2、ACVR2A、ACVR1B、SMAD2、SMAD3、SMAD4遺伝子の不活化でした。
P53シグナル伝達経路
P53シグナル伝達経路の不活化は、64%の遺伝子変異が顕著でない大腸がん、47%の遺伝子変異が顕著な大腸がんで起こっていました。TP53遺伝子の不活化は、59%の遺伝子変異が顕著でない大腸がん、17%の遺伝子変異が顕著な大腸がんで起こっていました。TP53遺伝子から転写翻訳されたタンパク質であるP53をリン酸化し活性化するタンパク質であるATMタンパク質の設計図であるATM遺伝子は、7%の遺伝子変異が顕著でない大腸がん、37%の遺伝子変異が顕著な大腸がんで不活化されていました。TP53遺伝子とATM遺伝子の不活化にも相互に排他的な傾向がありました。
1.国立がん研究センター がん情報サービス>それぞれのがんの解説>大腸がん
https://ganjoho.jp/public/cancer/colon/index.html
2.国立がん研究センター内科レジデント編、がん診療レジデントマニュアル、第8版、医学書院、2019年。
3.国立がん研究センターがん情報サービス>それぞれのがんの解説>遺伝性腫瘍・家族性腫瘍https://ganjoho.jp/public/cancer/genetic-familial/index.html
4.Cancer Genome Atlas Research Network. Comprehensive molecular characterization of human colon and rectal cancer. Nature. 2012; 487: 330-337. doi: 10.1038/nature11252. https://www.nature.com/articles/nature11252
参照:2021年07月06日