肺は、体に酸素を取り入れ二酸化酸素を排出する働きをする臓器です。胸部の左右に1つずつあり、右肺は3つ、左肺は2つの肺葉に分かれています。気管が左右の主気管支に分かれて左右の肺に入る部分を肺門、肺の本体部分を肺野と言います。気管支の先端部分には、小さな袋状の構造をしている肺胞が無数にあります。
肺がんは、気管支や肺胞の細胞ががん化したものです。
肺がんは、組織型によって非小細胞肺がんと小細胞肺がんに分けられます。非小細胞肺がんは、さらに腺がん、扁平上皮がん、大細胞がんに分けられます。非小細胞肺がんは、小細胞肺がんに比べて発生頻度が高く、中でも腺がんが最も発生頻度が高くなっています。小細胞肺がんは、非小細胞肺がんと比べて増殖速度が速くかつ転移しやすいという特徴があります。非小細胞肺がんでは、遺伝子変異検索や免疫学的因子(PD-L1)の検索が治療方針の決定に極めて重要です。
目次
肺がんのリスクファクター
喫煙、職業的暴露(アスベスト、ラドン、ヒ素、クロロメチルエーテル、クロム酸、ニッケルなどの有害化学物質)、大気汚染(特にPM2.5:2.5ミクロン以下の微小浮遊粒子)などが肺がんになるリスクを高めると考えられています。
肺腺がんに関係する遺伝子
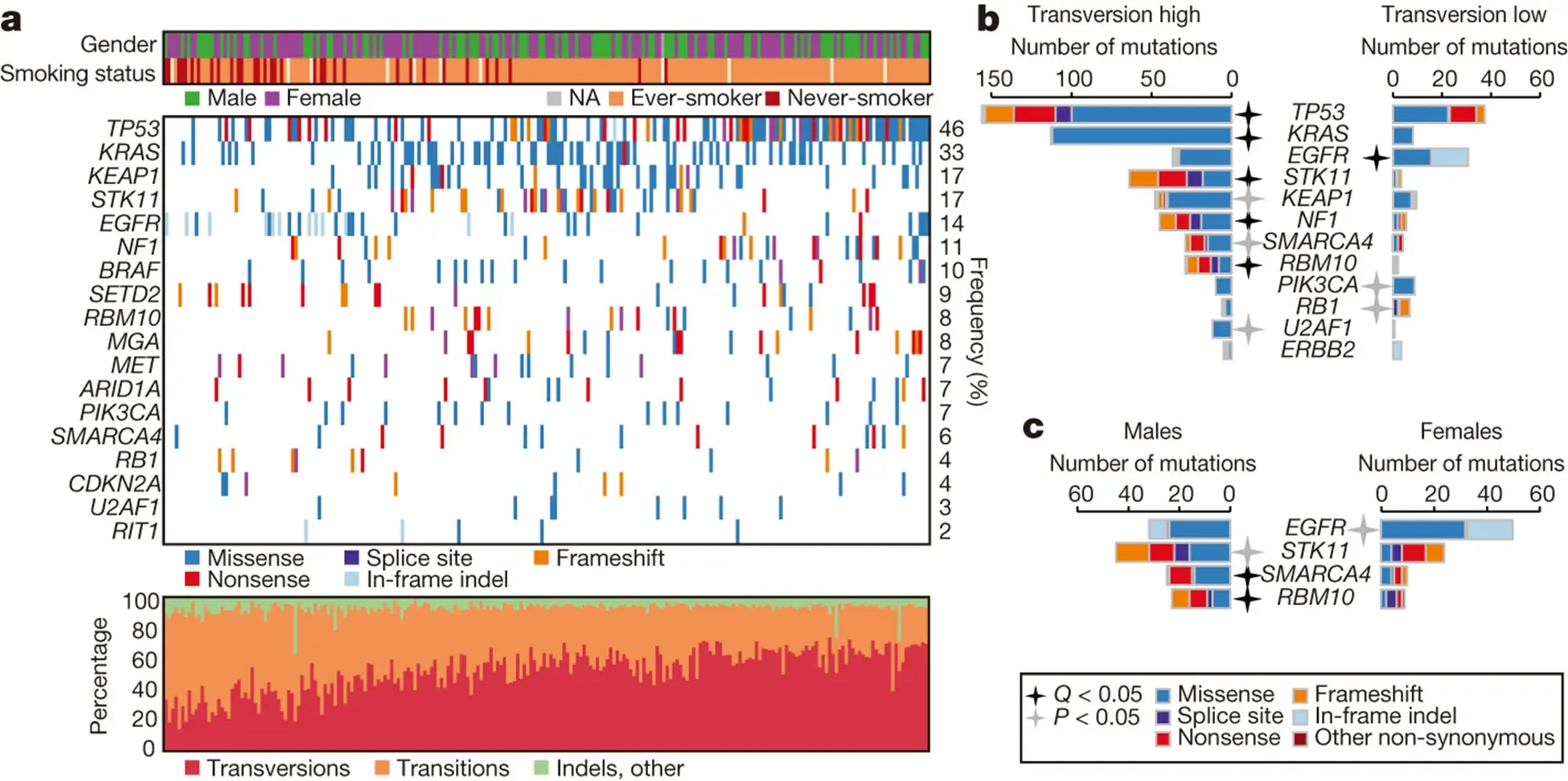
上の図は、230人の肺腺がんにおける遺伝子の変異を調べた結果です。
図aにおいて、上段に各患者様の性別を緑色(男性)と紫色(女性)の縦筋で示しています。その下には喫煙経験者をオレンジ色、喫煙非経験者を赤色で示しています。
3段目の四角に各患者様について変異した遺伝子を変異が多く見られた順に並べています。遺伝子の変異にはいろいろなパターンがあり、色分けして示しています。
DNAの塩基(アデニン、グアニン、シトシン、チミン)配列に蓄えられた遺伝子の情報は、メッセンジャーRNAの塩基(アデニン、グアニン、シトシン、ウラシル)配列に転写され、タンパク質のアミノ酸配列に翻訳されますが、 青色のMissenseとはアミノ酸が変わる変異を、赤色のNonsenseとはタンパク質合成が途中で止まる変異を示します。メッセンジャーRNAの塩基配列には、タンパク質のアミノ酸配列に翻訳される部分(エクソン)と翻訳されない部分(イントロン)がありますが、メッセンジャーRNAが翻訳される前にはイントロンが取り除かれエクソンが結合する必要がありますが、この過程をメッセンジャーRNAのスプライシングと言います。
紫色のSplice site
紫色のSplice siteとは、このRNAスプライシングを指示する塩基配列に起こった変異です。メッセンジャーRNAの塩基は3つで1種類のアミノ酸を指示し、この3つの塩基の読み枠をコドンと言います。
水色のIn-frame indel
水色のIn-frame indelとは、コドンを変化させない3の倍数の塩基の挿入や欠失を言います。
オレンジ色のFrameshift
オレンジ色のFrameshiftとは、コドンを変化させる3の倍数でない塩基の挿入や欠失を言います。46%の患者様にTP53の変異が見られました。KRAS(33%)と EGFR(14%)の変異は互いに異なる患者様に見られました。その他、KEAP1(17%)、STK11(17%)、NF1(11%)、BRAF(10%)の変異が10%以上の患者様に見られました。
DNAの塩基
DNAの塩基(アデニン、グアニン、シトシン、チミン)は、比較的大きな互いに構造が似ているプリン塩基(アデニン、グアニン)と比較的小さく互いに構造が似ているピリミジン塩基(シトシン、チミン)に分けられます。1塩基が置換する点変異には12通りありますが、プリン塩基とピリミジン塩基間の変異(8通り)を塩基転換(Transversions)、プリン塩基同士或いはピリミジン塩基同士の変異(4通り)を塩基転位(Transitions)と言います。
まとめ
図aでは、右側に喫煙経験のある患者様、左側に喫煙経験のない患者様が多いですが、下段の四角に示されているように、喫煙経験のある患者様では赤色で示した塩基転換(Transversions)が多く、喫煙経験のない患者様ではオレンジ色で示した塩基転位(Transitions)が多いという結果が得られました。
さらに図bに示されているように、塩基転換(Transversions)が多い患者様ではTP53、KRAS、RBM10等の遺伝子の変異が多く、塩基転位(Transitions)が多い患者様ではEGFR等の遺伝子の変異が多いことも分かりました。図cに示されているように、遺伝子の変異には性差があり、EGFR遺伝子の変異は女性に多いが、RBM10等の遺伝子の変異は男性に多いと言う結果も得られました。
肺扁平上皮がんに関係する遺伝子
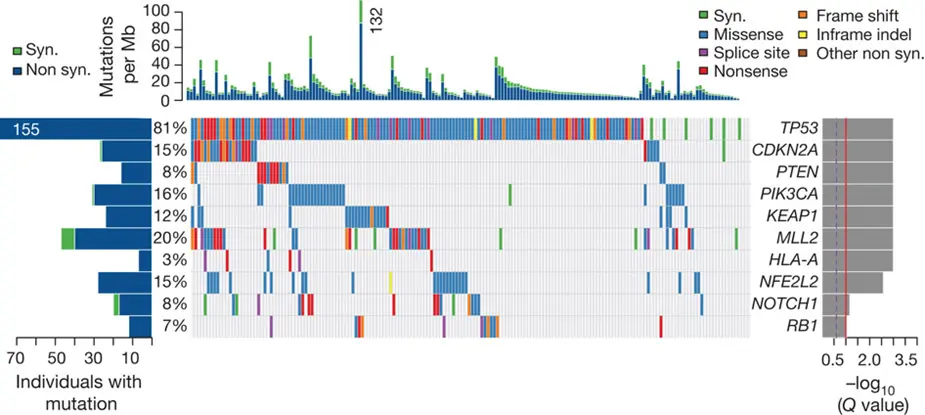
上の図は、178人の肺扁平上皮がんのがん組織における遺伝子の変異を調べたものです。
各患者様のデータは、中央の四角にどの遺伝子にどのような変異があったのかを色分けした縦長の棒で示しています。
上段のヒストグラムには各患者様のがんにおけるタンパク質のアミノ酸の配列を変えない変異(Syn.、緑色)と変える変異(Non syn.、青色)の割合を示しています。
各患者様の遺伝子の変異の種類については、タンパク質のアミノ酸の配列を変える変異(Missense)を青色で、RNAスプライシングを指示する塩基配列に起こった変異(Splice site)を紫色で、タンパク質合成が途中で止まる変異(Nonsense)を赤色で、コドンを変化させる3の倍数でない塩基の挿入や欠失(Frameshift)をオレンジ色で、コドンを変化させない3の倍数の塩基の挿入や欠失(In-frame indel)を黄色で、その他のアミノ酸の配列を変化させる変異を紫色で示しています。
統計的解析の結果、TP53、CDKN2A (p16)、PTEN、PIK3CA、KEAP1、MLL2、HLA-A、NFE2L2、NOTCH1、RB1遺伝子に多くの変異が見られました。中でもTP53遺伝子には81%の患者様に変異が見られました。
TP53遺伝子は、DNAの修復や細胞増殖停止、アポトーシス(細胞の自死)などによる細胞増殖サイクルを抑制する機能を持つタンパク質の設計図となるがん抑制遺伝子の一つです。
CDKN2A (p16)は、細胞周期の調整に重要な役割を果たすタンパク質の設計図となるがん抑制遺伝子の一つです。酸化ストレスはDNAを直接傷害することによってがんの原因となると考えられていますが、
KEAP1とNFE2L2は細胞の酸化ストレス応答に関わるタンパク質の設計図となる遺伝子です。
NOTCH1は、扁平上皮細胞の分化に関わるタンパク質の設計図となる遺伝子です。このように、細胞の正常な増殖や分化に関わるタンパク質の設計図となる遺伝子の異常によりがんが生ずることが考えられます。
非小細胞肺がんに対する分子標的薬
日本の肺がん患者様では、53%の患者様にEGFR遺伝子の変異が、3.8%の患者様にALK融合遺伝子変異が、0.9%の患者様にROS1融合遺伝子の変異が、0.3%の患者様にBRAF遺伝子の変異があると報告されています(5)。
非小細胞肺がんでは、これらの遺伝子変異を標的とした分子標的薬があります。EGFR遺伝子変異陽性の患者様に対しては、ゲフィチニブ(商品名イレッサ)、エルロチニブ(商品名タルセバ)、アファチニブ(商品名ジオトリフ)、オシメルチニブ(商品名タグリッソ)等の分子標的薬が適応となる可能性があります。
ALK融合遺伝子陽性の患者様に対しては、アレクチニブ(商品名アレセンサ)、クリゾチニブ(商品名ザーコリ)、セリチニブ(商品名ジカディア)等の分子標的薬が適応となる可能性があります。ROS1融合遺伝子陽性の患者様に対しては、クリゾチニブ療法が適応となる可能性があります。BRAF遺伝子変異陽性の患者様に対しては、タブラフェニブ(商品名タフィンラー)とトラメチニブ(商品名メキニスト)の併用療法が適応となる可能性があります。
1.国立がん研究センター がん情報サービス>それぞれのがんの解説>肺がんhttps://ganjoho.jp/public/cancer/lung/index.html
2.国立がん研究センター内科レジデント編、がん診療レジデントマニュアル、第8版、医学書院、2019年。
3.Cancer Genome Atlas Research Network. Comprehensive molecular profiling of lung adenocarcinoma. Nature. 2014; 511: 543-50. doi: 10.1038/nature13385. Epub 2014 Jul 9. https://www.nature.com/articles/nature13385
4.Cancer Genome Atlas Research Network. Comprehensive genomic characterization of squamous cell lung cancers. Nature. 2012; 489: 519-25. doi: 10.1038/nature11404. https://www.nature.com/articles/nature11404#MOESM280
5.Motonobu Saitoet al. Gene aberrations for precision medicine against lung adenocarcinoma. Cancer Sci. 2016; 107: 713-20. doi: 10.1111/cas.12941. Epub 2016 May 25.
参照:2021年06月28日