こんにちは。川森です。
FDAからお薬の承認メールが届きましたので、情報をシェアさせていただきます。

You are subscribed to Oncology Drugs for U.S. Food and Drug Administration. This information has recently been updated, and is now available.
FDA approves fam-trastuzumab deruxtecan-nxki for HER2-positive gastric adenocarcinomas
https://www.fda.gov/drugs/drug-approvals-and-databases/fda-approves-fam-trastuzumab-deruxtecan-nxki-her2-positive-gastric-adenocarcinomas
HER-2陽性の乳がんの治療薬としてすでに認可されているトラスツズマブデルクステカン(fam-trastuzumab deruxtecan-nxki、エンハーツ、第一三共)が、HER-2陽性胃がんの治療薬として承認されました。
どのような患者様かというと、成人でHER-2陽性局所進行胃がんまたは転移のある胃がんですでにハーセプチンの治療歴のある患者様が対象です。
この承認は、多施設、マルチコホート、無作為オープンラベル臨床試験(DESTINY-Gastric01, NCT03329690)の結果に基づきます。126人のHER-2陽性で局所進行の胃がんまたは転移性胃がん患者でこれまでに少なくとも2種類以上の抗がん剤治療、ハーセプチン、fluoropyrimidineを含む抗がん剤かplatinumを含む抗がん剤を行った既往のある患者様を無作為にエンハーツ投与群とイリノテカンかパクリタキセル群に振り分けました。
効果は、全生存期間(overall survival, OS)で判定された。エンハーツ投与群は、12.5ヶ月、対照群は8.4ヶ月でした。エンハーツ投与は有意に生存期間を延長しました。
推奨される投与方法は、6.4mg/kg体重を静脈内注射し、3週間毎に胃がんの増悪または許容できない副作用が出現するまで行います。
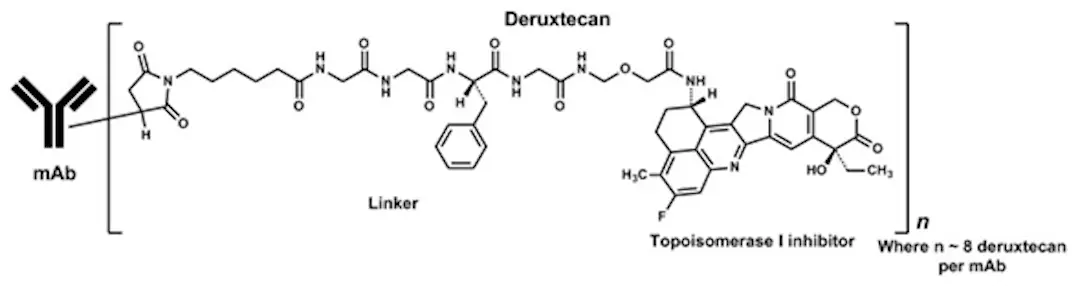
ちなみに、エンハーツの構造を上に示します。エンハーツは、抗体―薬物複合体(antibody-drug conjugate, ADC)と呼ばれるお薬です。
3つの構成成分からなり、
1)左のmAbと書いてあるのが、ハーセプチンに当たるHER-2に対する抗体の部分
2)topoisomerase I inhibitor(右側)
3)その2つをリンクしているDeruxtecanと呼ばれるリンカーで構成されています。
最近、このような抗体と抗がん剤、薬物をリンクさせて、抗体で腫瘍細胞を認識させ、抗がん剤で叩くというハイブリッド医薬品が増えています。
腫瘍細胞の特性を利用して腫瘍細胞だけを高濃度の抗がん剤で局所的にやっつけてくれると全身の副作用は軽減でき、効果が期待できるので、良い考えですね。